





















A era digital está avançando rapidamente e, com ela, a necessidade de conhecimento em tecnologias emergentes como a Inteligência Artificial (IA). Pensando nisso, o Sebrae SP,...



CAMPINAS – O Hopi Pride Festival 2024 marcou seu lugar no calendário de eventos LGBTQIA+ como um dos mais aguardados do ano. Com uma multidão de...
Introdução Hoje em dia, a função de Técnico de Manutenção de Máquinas e Equipamentos é uma das mais solicitadas no mercado de trabalho. Neste artigo, vamos...



Uma operação recente da Polícia Civil de Itu resultou na detenção de criminosos envolvidos no tráfico de drogas e na apreensão de uma quantidade expressiva de...
A função de um Consultor de Vendas é fundamental para diversas empresas. Seja em Indaiatuba – SP, ou em qualquer outro lugar, esse profissional é indispensável...
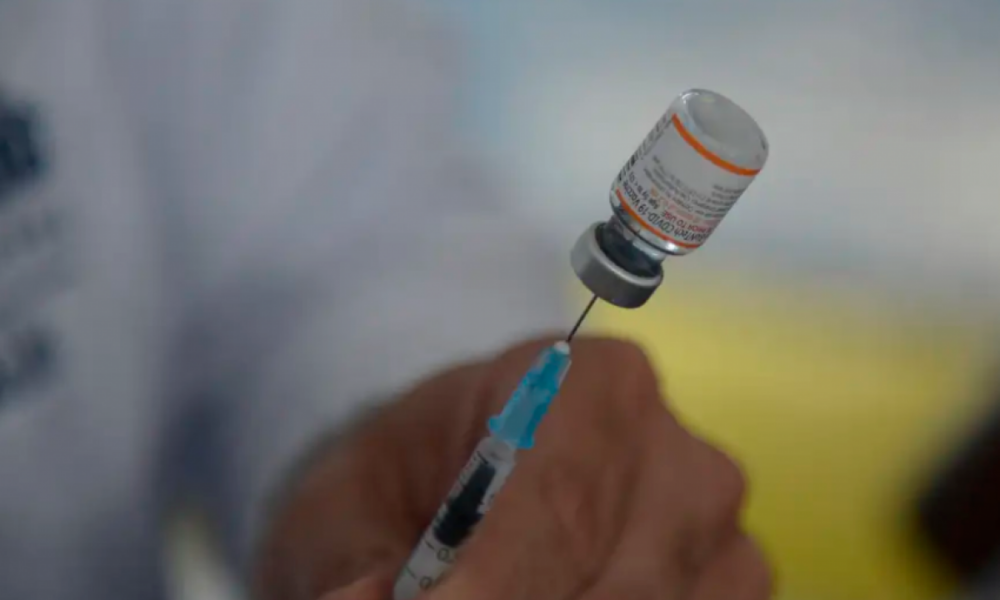
O Ministério da Saúde confirmou a aquisição de 12,5 milhões de doses da nova vacina contra COVID-19, produzida pela farmacêutica Moderna. O Início de Uma Nova...



Introdução No dia 22 de abril de 2024, o Brasil acordou com uma variedade de notícias que balançaram o país. Esse artigo buscará explorar a influência...



> ‘Os animais compartilham conosco o privilégio de ter uma alma.’ – Pitágoras A cidade de Itu, conhecida por sua rica história e belas paisagens, está...



> Postado em: 22 de abril de 2024 > Categoria do post: Assessoria de Imprensa / Notícias / Secretaria de Cultura A Prefeitura da Estância Turística...



— Introdução Na madrugada de um domingo, a tranquilidade da cidade de Hortolândia foi interrompida por uma notícia chocante. Um homem, conhecido como Jailson da Silva,...